Anatomia
Strain na Estenose Aórtica moderada
22 de junho de 2020Medida do anel tricúspide
25 de junho de 2020[vc_row type=”in_container” full_screen_row_position=”middle” scene_position=”center” text_color=”dark” text_align=”left” overlay_strength=”0.3″ shape_divider_position=”bottom” bg_image_animation=”none”][vc_column column_padding=”no-extra-padding” column_padding_position=”all” background_color_opacity=”1″ background_hover_color_opacity=”1″ column_link_target=”_self” column_shadow=”none” column_border_radius=”none” width=”1/1″ tablet_width_inherit=”default” tablet_text_alignment=”default” phone_text_alignment=”default” column_border_width=”none” column_border_style=”solid” bg_image_animation=”none”][vc_column_text]
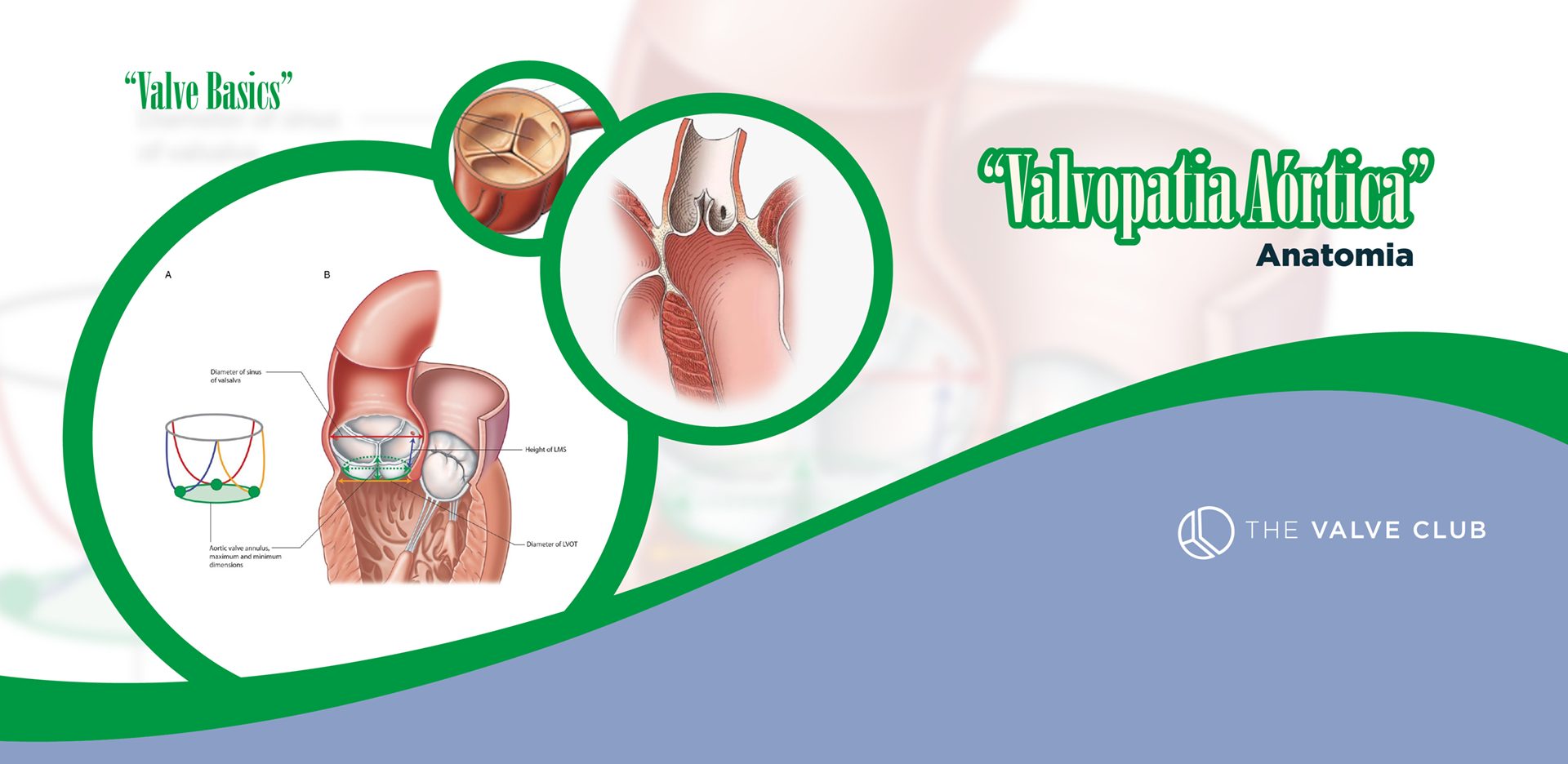
Anatomia
[/vc_column_text][vc_column_text]
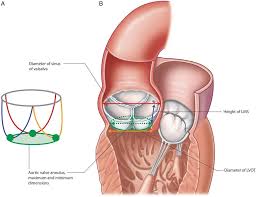
A valva aórtica é a parte inicial da raiz da aorta, formando um complexo valvar aórtico composto por:
- Seios de Valsalva
- Triângulos fibrosos intercalares (entre os folhetos)
- Três folhetos valvares
O plano de inserção dos folhetos marca o início da raiz da aorta e a junção sinotubular separa essa raiz da aorta ascendente. A porção posterior do anel aórtico está em íntimo contato com o anel e orifício mitral e o septo interventricular. Assim, cerca de 2/3 da porção posterior está em contato com o septo interventricular e 1/3 está com a fibrosa mitro-aórtica (FIMA).
Como descrito, a valva aórtica é composta por 3 folhetos com implantação semilunar, ao longo do anel. A borda livre de cada um se curva ligeiramente a partir das comissuras e apresenta discreto espessamento nas pontas, ponto esse chamado de “Arantius”. Cada um dos folhetos é identificado pela relação com os óstios das coronárias em: coronariano direito, coronariano esquerdo e não coronariano.
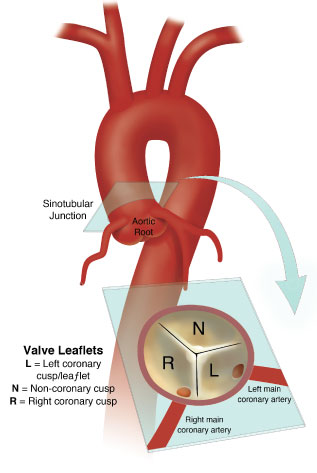
Os seios de Valsalva são áreas de expansão da parede da raiz da aorta, sendo separados uns dos outros pelos triângulos fibrosos. Quando os folhetos estão abertos durante a sístole não há obliteração dos óstios coronários por causa dessas expansões. Formam-se vórtices de fluxo nessa região garantindo perfusão coronariana. Em caso de ausência desses triângulos, o seio perde a conformação de coroa e essa alteração é correlacionada com quadros de estenose aórtica.
Virtualmente, o ponto que liga o local mais baixo da implantação de cada folheto, forma o anel valvar aórtico, que tem conformação discretamente elíptica, com medida tridimensional em torno de 4,0 ± 0,8 cm2. Diante dessa conformação espacial, a medida tridimensional, seja pela ecocardiografia ou pela tomografia é muito mais fidedigna e reprodutível do que a bidimensional obtida pela ecocardiografia transtorácica comum.
Adaptação Ventricular
Em todas as valvopatias com repercussão hemodinâmica, o ventrículo esquerdo passa a lidar com determinadas sobrecargas. Dessa forma, o ventrículo lança mão de três mecanismos básicos para lidar com isso:
- Mecanismo de Frank-Starling
- Sistemas Neuro-Humorais adrenérgicos
- Remodelamento de câmara
Vale ressaltar nesse ponto da discussão que hipertrofia e remodelamento não são sinônimos. A hipertrofia significa aumento de massa, enquanto o remodelamento, significa mudança na geometria e/ou volume. Portanto, devemos entender que os termos podem coexistir, mas não necessariamente.
Na vigência de uma estenose aórtica, surge um gradiente sistólico que o ventrículo esquerdo deve gerar a mais do que o necessário para vencer a barreira anatômica para a ejeção do sangue. Isso leva a uma resposta biológica de hipertrofia concêntrica e/ou remodelamento do ventrículo esquerdo com formação de sarcômeros em paralelo, espessamento da parede e aumento da massa. Como trata-se de um processo adaptativo, é de se esperar que a hipertrofia vá até o nível em que o stress de parede volte ao normal. No entanto, em alguns pacientes, esse processo não consegue manter o adequado equilíbrio e falha.
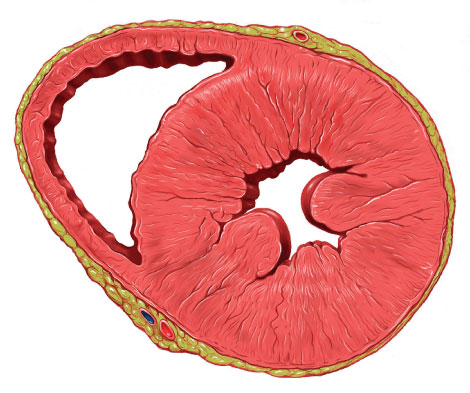 Pacientes com disfunção ventricular esquerda apresentam um balanço hemodinâmico com elevada pós-carga para o grau de hipertrofia, que não ocorreu na proporção que deveria. O oposto também pode ocorrer, com elevada hipertrofia frente a determinada elevação da pós-carga. É o caso dos pacientes com valva aórtica bivalvar congênita e nas mulheres idosas. Nesse grupo de pacientes, mesmo com uma fração de ejeção preservada, podemos experimentar graus diversos de disfunção diastólica e queda no padrão do “strain” ventricular assinalando a presença de doença.
Pacientes com disfunção ventricular esquerda apresentam um balanço hemodinâmico com elevada pós-carga para o grau de hipertrofia, que não ocorreu na proporção que deveria. O oposto também pode ocorrer, com elevada hipertrofia frente a determinada elevação da pós-carga. É o caso dos pacientes com valva aórtica bivalvar congênita e nas mulheres idosas. Nesse grupo de pacientes, mesmo com uma fração de ejeção preservada, podemos experimentar graus diversos de disfunção diastólica e queda no padrão do “strain” ventricular assinalando a presença de doença.
Pacientes que apresentam insuficiência aórtica experimentam não apenas sobrecarga de volume, mas uma sobrecarga mista. Esses pacientes apresentam também elevada pós-carga devido a um volume sistólico elevado frente a uma resistência vascular periférica aumentada pelo stress adrenérgico crônico. Assim, de todas as lesões valvares, a insuficiência aórtica é a que apresenta maior massa do ventrículo esquerdo. Há uma ativação do processo de produção de miofilamentos com uma redução de sua degradação que era para ser a fisiológica.
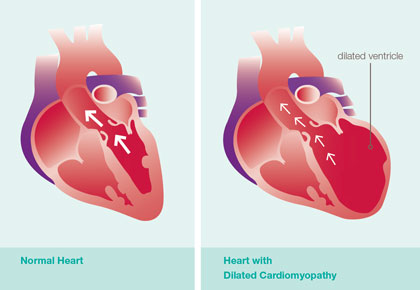
Em alguns modelos animais, o estudo do miocárdio mostrou que o aumento da matriz extracelular parecia atrapalhar a dinâmica contrátil, podendo ser uma das explicações para a queda da fração de ejeção nesses casos. No entanto, o procedimento cirúrgico de correção da valvopatia fazia retornar a função contrátil, podendo ser explicada pela regressão dessa matriz extracelular frente a uma redução importante da pós-carga no pós-operatório.
A partir desse momento, vamos separar a discussão em dois grandes grupos de acordo com a disfunção valvar específica, entre estenose e insuficiência valvar aórtica.
[/vc_column_text][vc_column_text]Literatura sugerida:
1 – Otto CM, Bonow RO. A Valvular Heart Disease – A companion to Braunwald’s Heart Disease. Fourth Edition, 2014.[/vc_column_text][image_with_animation image_url=”6177″ alignment=”center” animation=”Fade In” border_radius=”none” box_shadow=”none” max_width=”100%”][/vc_column][/vc_row]